藥華藥(6446)今(15)日受邀參加法說會,說明2024第二季財報、近期營運重點及未來展望。
2024第二季財報重點
藥華藥第二季營收23.0億元,季增39.50%,年增82.35 %,已連續五季度創新高。第二季本業獲利達4.4億元,季增2,417%,較去年同期增加8.5億元;第二季淨利達6.8億元,季增106%,較去年同期增加8.8億元;基本每股盈餘(EPS)達 2.09元,均創新高。繼今年第一季首次達成單季本業獲利的里程碑後,第二季本業獲利進一步大躍升,並有持續成長趨勢。
藥華藥旗下治療真性紅血球增多症(PV)新藥Ropeginterferon alfa-2b(簡稱Ropeg, 即P1101)全球銷售持續成長,值得關注的是,相較營收季增近40%,費用僅季增8%,更較去年同期降低,主要為控管管理及銷售費用。
藥華藥上半年累計營收39.6億元,較去年同期成長83.97%。同時在嚴謹管控費用的努力下,費用與去年同期相比較低。上半年本業獲利大幅度成長到4.6億元,較去年同期增加近16億元;上半年淨利達10.1億元,較去年同期增加近20億元;EPS達3.05元。充分突顯新藥公司業績的爆發力,以及高獲利能力。
公司表示,營收及獲利均呈成長趨勢,並維持高毛利率。以目前趨勢,營收有望持續維持逐季成長;再配合控管營運支出,在嚴謹管控費用且銷售能力提升下,獲利表現將會愈來愈佳。
藥華藥本月5日公布7月營收8.8億元,已連續三個月創新高,年增97.31%,維持強勁年成長率。今年累計至7月營收已達48.4億元,年增86.26%。
近期營運重點:隨全球營運規模擴大獲利快速成長
美國市場方面,營收持續加速成長,開立Ropeg處方的新醫師持續增加。除學術醫院外,社區醫院市場增長強勁,積極推動業績成長。藥華藥美國子公司自今年初重組行銷領導團隊,近期又新禮聘專長法遵的法務主任,有望使營收持續維持逐季增長的趨勢。
日本市場方面,銷售持續成長。公司表示,日本醫病關係非常密切,患者停止用藥的比例十分低,與藥華藥日本團隊持續進行病患支持的服務、尋找PV潛在患者,並積極推動患者進行JAK2突變基因的檢測有關。不僅與病友團體設立基金以提供經濟補助給使用Ropeg的患者,也設立網站讓患者可以自我診斷,均非常有助於患者及早進行治療,促進提升使用Ropeg的病人數和施打高劑量的Ropeg,擴大市場。
中國市場方面,Ropeg於6月28日獲中國藥監局核准用於PV,為第一且唯一獲中國核准用於PV藥物,等同於順利搶到今年進入中國國家基本醫療保險門票。藥華藥中國團隊已於7月中申請Ropeg進入醫保,最快可於今年年底取得醫保藥價,讓更多中國PV病患受惠。因大陸的特殊藥價政策,公司目前將先聚焦在中國各大醫院進行Ropeg的自費銷售,並將持續洽談適合的銷售合作對象。
另外,藥華藥韓國團隊今年再次申請Ropeg納入當地健保,預計明年年底前取得健保藥價,造福更多韓國PV病患;Ropeg也已於今年5月底取得新加坡PV藥證,公司依計畫積極進行Ropeg於新加坡上市之銷售業務及行銷活動,已申請將Ropeg列入當地癌藥目錄,預計最快今年9月正式於新加坡上市,進軍東南亞市場。
未來展望:獲利成長與創新研發並進持續擴大研發能量
- 照計畫力拚新藥研發
- 增加Ropeg新適應症
有關擴展Ropeg新適應症進度,用於原發性血小板過多症(ET)的全球第三期臨床試驗(SURPASS-ET)於2023年10月收案完成,共收入174個 ET患者,預計2024年底到2025年初可完成主要療效指標數據收集,2025年開始申請各國藥證,包括美國、中國及日本等國,最快2025年底取證,現正投入行銷前準備。
而Ropeg用於早前期原發性骨髓纖維化(Early PMF)的全球第三期臨床試驗(HOPE-PMF),目前正在與美國FDA討論全球三期臨床試驗計畫。
Ropeg於日本進行用於治療復發或難治性成人T細胞白血病/淋巴瘤(ATL)的第二期臨床試驗,已於今年7月正式收入第一位病患。藥華藥將持續多元發展,拓展Ropeg的治療領域,造福全球更多患者。
- 其他臨床試驗進度
Ropeg以外的新藥臨床試驗進度亦進展順利,長效型顆粒性白血球生成素(PEG-GCSF, 即P2203)在台灣進行的第一期臨床試驗預計於8月下旬收入第一位受試者。
在運用TCR-T細胞療法治療實體腫瘤方面,則是預計今年申請進入新藥臨床試驗(IND)。
- 擴大研發能量
藥華藥持續創新研發,為擴大研發能量及發展多元產品線,藥華藥台北研發中心據點自南港軟體園區的13樓擴充至18樓和19樓;同時,更進一步擴充至國家生技園區及台北生技園區,未來可成為進行細胞療法與生物藥研發、試製及GMP生產的廠房。
位於波士頓的創新研發中心著重開發同類最優(BiC)和同類第一(FiC)療法、積極發掘策略合作夥伴,持續主動探索創新研發項目以拓展產品線。
全球供應鏈進度
藥華藥台中廠第二條產線已擴建完成,近期啟動製程確效,產能倍增可供應2萬多病患。此外,為擴充產能,竹北廠工程持續順利進行中,預計2026投產,產能可供應超過10萬名病患。
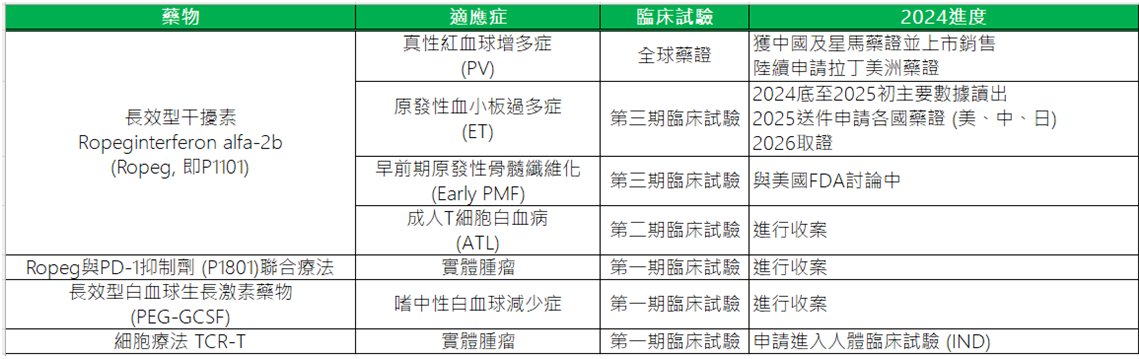
▲2024臨床試驗進度列表





















