生技股東生華 (8432)於上週五(10/11)公告今年8月台灣首篇液態切片(胸水)研究成果成功發表於國際期刊,在10月也成功獲得台灣衛生福利部核准,成為首例通過「實驗室開發檢測與服務」(Laboratory Developed Tests and Services, LDTs)的液態切片(體液)NGS 基因檢測,在次世代基因檢測(NGS)領域再次創下里程碑!激勵今(14)日股價盤中大漲逾7%,終場收盤價報65.7元,大漲3.2元、5.12%,漲逾半根漲停板,成交量報456張。
東生華表示,隨著台灣於今年2月落實 LDTs 認證,經過嚴謹的數據審查和技術驗證,於本月正式通過該項認證。這不僅提升東生華在精準醫療分子檢測領域的競爭力,也確保為患者提供的基因檢測服務具有高度的可靠性和準確性。
衛生福利部於10月8日發函核准確認通過三項檢測項目,包括「癌克準-100 組織切片」、「癌液準-100 液態切片(體液)」及「癌液準-100 液態切片(血液)」。其中,癌液準-100 液態切片(體液)是專門獨立針對癌症患者胸水、腹水及腦脊髓液進行 NGS 基因檢測產品,為台灣首例通過 LDTs 審查許可。
癌液準-100 液態切片(體液)突破了傳統細胞塊檢測的局限。相較於傳統方法只能檢測到約 51% 的癌症驅動基因突變,我們的液態切片技術識別出超過 92% 的突變,涵蓋常見的 EGFR、ALK、ROS1 等基因,以及罕見的非熱點區域突變,如 EGFR、KRAS、MET exon 14 跳躍突變、NRAS、BRAF 和 ERBB2 擴增等。
癌液準-100 液態切片(體液)在靈敏度和檢測範圍上顯著優於傳統檢測。此外,液態切片相對於組織活檢具備更低的侵入性,且能在平均7天內提供報告,大幅縮短了檢測時間,提供了快速且精準的臨床決策依據。目前,該技術已在台灣多家醫學中心完成臨床驗證,累計檢測超過1000例。
東生華的液態切片產品不僅為癌症基因檢測帶來了新突破,也在精準醫療領域邁出了重要的一步。這項成果讓台灣在國際上更具競爭力,我們將繼續努力,推動更多創新技術,期望為醫療團隊和患者提供更快、更精準的診斷工具。未來,東生華會持續在這個領域深耕,讓更多人能夠從中受益,共同迎接精準醫療的新時代。
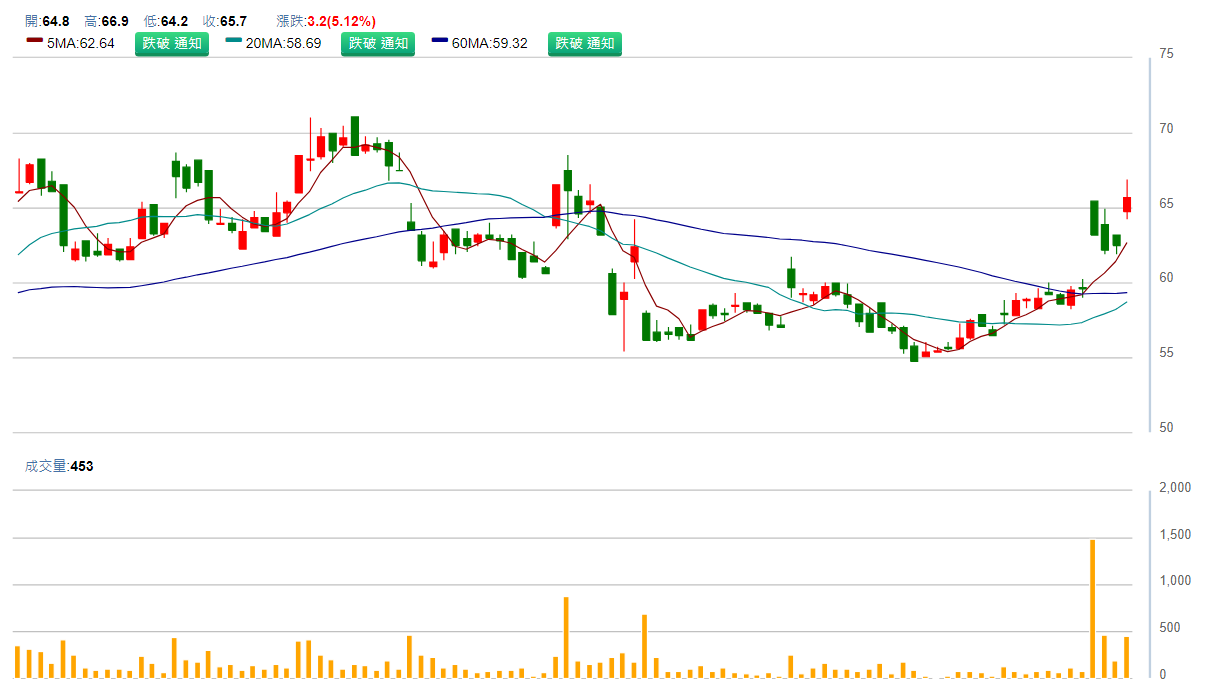
▲東生華(8432) 日K圖 (來源:CMoney)























