昨(11)日晚間,康霈*(6919)公告旗下全球首創透過誘導脂肪細胞凋亡來精準減少注射部位脂肪的大範圍局部減脂注射劑新藥CBL-514,由美國FDA、澳洲TGA核准,由12家試驗中心,共107位受試者參與進行的Phase 2b臨床試驗解盲順利達標,超過8成的受試者腹部脂肪顯著減少,顯示CBL-514可望於2025年進入全球三期樞紐試驗,有機會成為全球第一個可用於大範圍局部減脂的新藥。今(12)日康霈*股價開盤一字鎖,要買等明日拚手速!
反觀順藥(6535)公布缺血性腦中風新藥LT3001中國大陸第二期臨床試驗解盲成功,卻連吞六根跌停板,其差異在於未公告對應的療效P值。
兩者差異很明顯在於「療效」,LT3001第二期試驗結果,順藥僅說「安全」但高劑量組、低劑量組與安慰劑組並未有明顯差異,但卻說足以支持接下來的試驗,試驗時間未出來,這段空窗期引發市場許多不安因素,導致被倒貨,大股東晟德(4123)趕緊提10億元救火才止跌,不過今日股價仍在191元附近徘迴,對比近期股價400元的高點還有不小的差距。
康霈生技的新藥CBL-514是全球首個專用於大範圍局部減脂的注射劑,透過誘導脂肪細胞凋亡,實現非侵入性脂肪減少,將減少傳統抽脂手術造成的生命安全風險,對於希望減肥的人是一大福音。康霈生技表示,根據試驗數據,在具有完整數據的受試者群組(FAS)中,有76.7%的受試者腹部脂肪堆積等級改善至少1個等級,對比安慰劑組的18.9%,療效表現顯著(p=0.00004);符合試驗規範的受試者群組(PP)則改善率更高,達81.8%。此外,治療後12週,32%的受試者腹部脂肪堆積等級改善至少2個等級,安慰劑組則為0%(p=0.00122)。
MRI數據進一步驗證CBL-514的療效,康霈生技分享,治療後4週,CBL-514組的腹部皮下脂肪厚度平均減少27.1%(p<0.00001),值得注意的是,58.8%的受試者僅需接受一次療程,即可達到顯著改善,顯示該藥物的快速見效和便捷性。
至於安全性方面,康霈生技說,CBL-514表現良好,受試者完成最多4次療程後,主要不良事件為輕度至中度的注射部位反應,整體耐受度佳,顯示該藥物在非手術局部減脂領域具有高應用潛力。
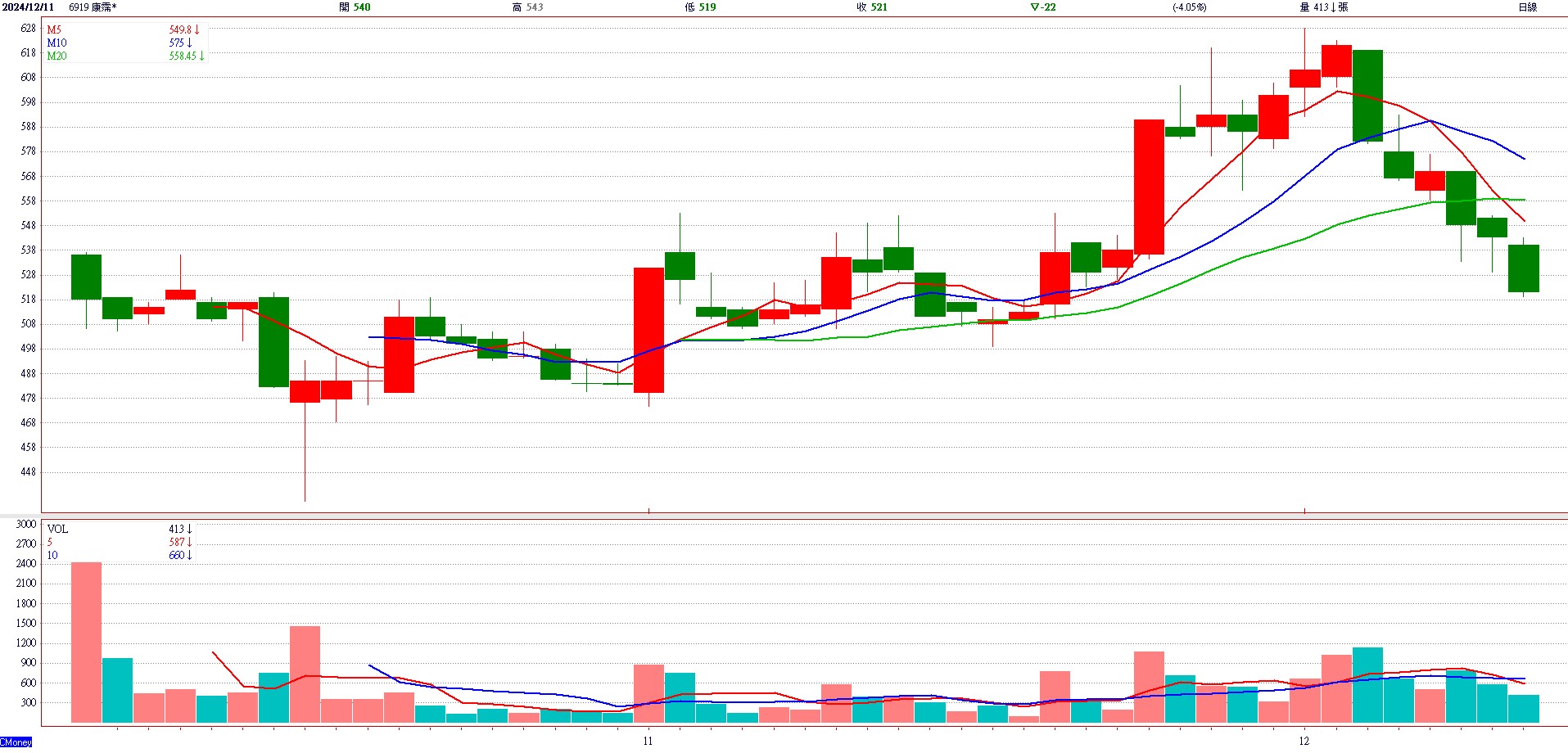
▲康霈*(6919) 日K圖 (來源:CMoney)
完成問卷 就送10天日報免費看👀https://forms.gle/nwypdLCdnVmytGRz7
點我加理周寶LINE好友🔥最新看漲訊息報給你知 https://lin.ee/EDu8u6q